▉ 摘要
随着抗HER2靶向治疗的发展,人类表皮生长因子受体2(HER2)扩增的乳腺癌(BC)患者的临床疗效也在不断的提高。然而,患者在治疗后可能会出现疾病复发,并在转移的情况下出现疾病进展。
在当前免疫治疗药物不断发展的时代,对抗HER2肿瘤细胞的免疫反应的理解也在不断提高。Trastuzumab治疗促进了HER2过表达的BC患者的NK细胞的激活,这表明短期曲妥珠单抗治疗的疗效,不仅与对HER2直接抑制有关,而且也可能与抗体依赖的细胞毒性相关(ADCC)。但是,在疾病复发或进展的患者中,ADCC可能会受到一些因素的影响,如FcgRIIIa多态性和免疫抑制环境等因素。因此,目前很多正在研究的药物都是希望通过增强ADCC效应来增加靶向HER2的抗体治疗BC的效果。本文章主要对目前在HER2阳性BC治疗领域的一些增强ADCC效应的策略进行了汇总和介绍。
抗体依赖性细胞毒性(ADCC)是一种细胞介导的免疫反应,其通过特定的抗体(Abs)附着在细胞上并利用免疫细胞引发细胞死亡。它是体液免疫反应的一个主要方面,可以限制和遏制感染。通常情况下,抗体结合NK细胞表面的FcγRs,从而激活NK细胞产生ADCC效应。NK细胞膜上最有特色的CD16(FcγRIII)。一旦FcγR与IgG的Fc片段结合细胞就会释放不同的细胞毒性分子,引起靶细胞的死亡。FcγRs由三个不同类别组成。FcγRI(CD64)、FcγRII (CD32) FcγRIIa和FcγRIIb,以及FcγRIII (CD16) FcγRIIIa和FcγRIIIb。
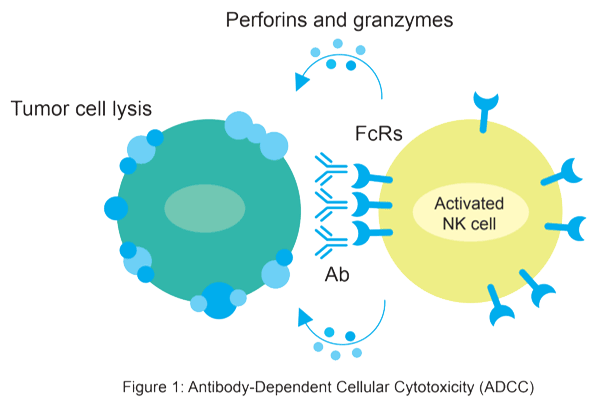
https://www.genscriptprobio.com/add-adcc-cdc-adcp.html
FcγRI是一种高亲和力的受体,可以与单体IgG结合。FcγRII和FcγRIII对单体分子表现出较低的亲和力并与多聚体免疫复合物有较强的亲和力。FcγRIIbs在单核细胞/巨噬细胞和多核细胞上诱发抑制性信号。相反,FcγRIIa和FcγRIIIa是活化性结合受体并在单核细胞、巨噬细胞和NK细胞上表达。尽管大多数免疫细胞同时表达激活性和抑制性的FcγRs,但NK细胞是独特的,因为它只构成性地表达激活型低亲和力FcγRIIIa。同时也有研究表明,外周血中的slant单核细胞也具有较高的ADCC效应。
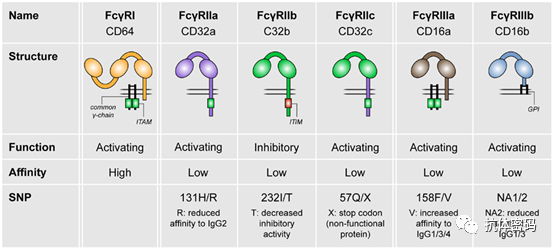
ADCC作为各种mAbs的治疗效果的作用已经在临床前模型中得到测试,并在患者中得到验证,目前已知ADCC是利妥昔单抗(抗CD20)、西妥昔单抗(抗EGFR)和曲妥珠单抗等抗体促进肿瘤治疗的的主要作用机制之一。伴随着细胞毒性颗粒和穿孔蛋白等细胞毒性颗粒的同时,NK细胞还释放了炎症细胞因子,如IFN-g和TNF-a,这种机制被称为抗体依赖的细胞因子释放(ADCR)。曲妥珠单抗治疗促进了NK细胞的激活,在HER2过表达的BC患者中,曲妥珠单抗的疗效与ADCC机制有关。NK细胞和肿瘤细胞之间由抗HER2抗体介导的相互作用,以及由ADCC诱导的促炎症环境可以调控其他免疫细胞群,导致治疗性Abs的 “疫苗接种效应”。
众所周知,NK细胞的活力是由细胞表面的抑制剂和激活剂受体产生的信号的平衡来处理的。不同的增强NK细胞激活的策略可以结合起来以增强其ADCC效应。由于NK细胞也可以通过释放细胞因子触发其他免疫过程。它们提供了一个启动其他免疫反应的环节。一研究结果表明,细胞因子、免疫疗法和针对NK细胞受体的Abs或具有激活和抑制功能的共受体的组合方法都能达到增强ADCC的效应(下图)
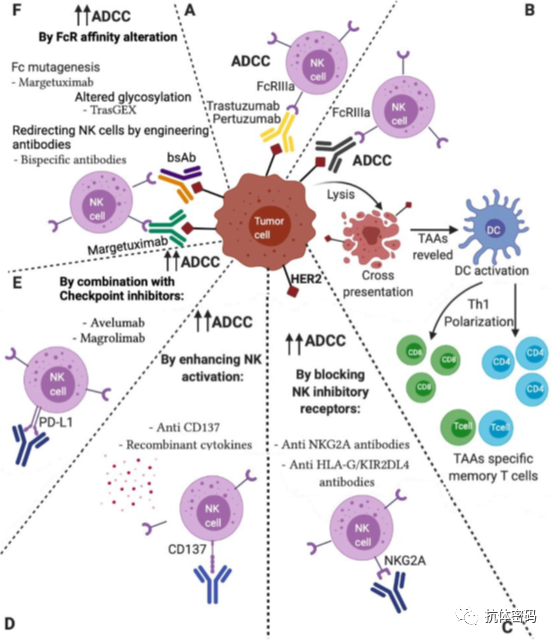
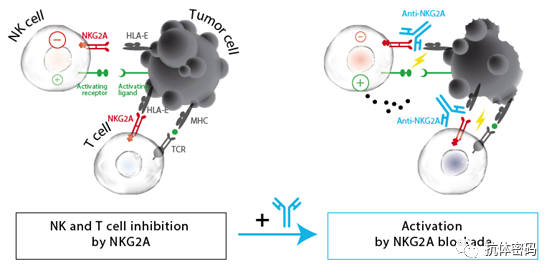
与T细胞不同,NK细胞的识别不是由抗原特异性的调节,而是通过许多激活和抑制性受体传达的信号来介导的。这种平衡决定了NK细胞的激活或抑制。NK细胞有一个抑制性受体的复杂排列。杀伤性免疫球蛋白(Ig)样受体(KIRs),识别不同等位基因组的HLA-A/B/C分子的不同等位基因,而CD94-NKG2A识别HLA-E(一种属于HLA-Ib的非多态性分子)。NK细胞通过高度特异性的受体识别主要组织相容性复合物(MHC)I类分子,并由此抑制NK细胞的激活。因此,通常发生在癌细胞中的MHC-I分子和抗原呈递的丧失,会诱导NK细胞介导的目标细胞的裂解。
抗NKG2A抗体增强ADCC
Monalizumab(IPH2201)是一种第一类免疫检查点抑制剂,针对NK细胞和肿瘤浸润性CD8þ T细胞上表达的NKG2A受体。Monalizumab通过阻断NKG2A和经常在一些恶性肿瘤中过量表达的HLA-E之间的相互作用,可恢复由这些细胞介导的广泛的抗肿瘤反应。Monalizumab可以同时作用于T细胞和NK细胞。同时也作用于肿瘤浸润性免疫细胞。因此,它可以和其它抗体联合使用,增强其他治疗性抗体药物的细胞毒性潜力。鉴于其与西妥昔单抗联合使用的结果令人鼓舞,一项名为MIMOSA II期临床试验正在评估Monalizum和曲妥珠单抗联合治疗对转移性或局部无法治愈的HER2阳性BC患者的疗效。
抗HLA-G/KIR2DL4的阻断作用
肿瘤细胞中HLA-G的表达已被确定为BC对曲妥珠单抗抗性的一个关键媒介。当HLA-G不与KIR2DL4作用时,KIR2DL4会促进ADCC效应,并与IFN-γ产生途径形成一个调节回路—其中IFN-γ通过JAK2/STAT1信号上调KIR2DL4,然后KIR2DL4与Fcγ受体协同作用,增加NK细胞分泌IFN-γ。因此,阻断HLA-G/KIR2DL4相互作用可以改善体内HER2阳性BC对曲妥珠单抗治疗的敏感性。
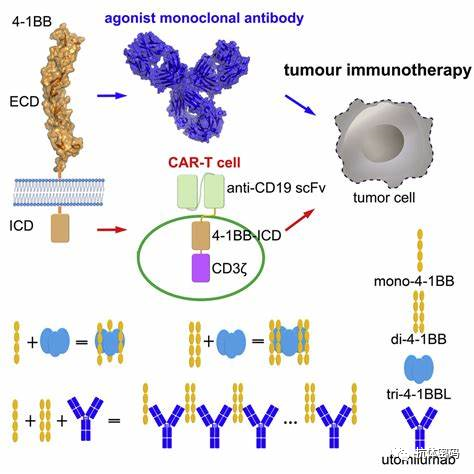
CD137/4-1BB
4-1BB,也被称为CD137,是一种刺激性免疫受体,是TNF受体超家族的成员。主要表达在活化的CD4þ和CD8þ T细胞、活化的B细胞和NK细胞上。4-1BB在免疫反应调节中发挥着重要作用,鉴于它在TILs上的表达因此被认为是癌症免疫治疗的一个有希望的靶标标。激活后,它能促进T和NK细胞的增殖、细胞因子的产生和细胞溶解活性的提高。
Utomilumab是一种完全人源化的IgG2 mAb,与4-1BB结合并阻碍对内源性4-1BBL的结合。一项正在进行中临床试验评估了utomilumab与TDM-1或曲妥珠单抗治疗HER2阳性BC患者的剂量和安全性(NCT03364348)。
重组细胞因子
NK细胞有一系列的细胞因子受体用于NK细胞的发展、内态平衡以及功能的发挥。因此,可能也可以通过重组细胞因子来调节NK细胞来加强ADCC效应。
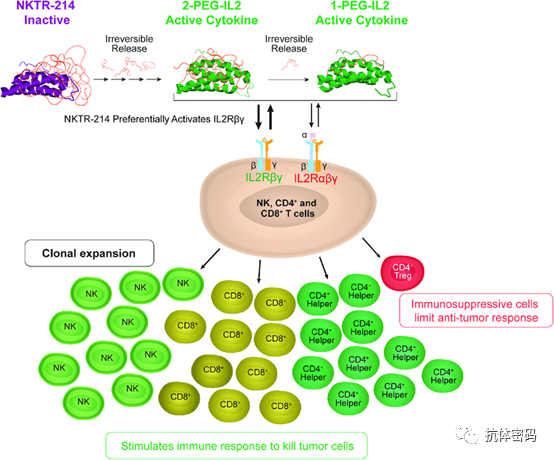
IL-2
IL-2是一种免疫刺激性细胞因子,可以增强NK细胞的反应。IL-2皮下给药可使循环中的NK细胞的增加约10倍的绝对数量,并增强其对几个BC靶点的作用。然而,迄今为止,这种免疫激活的非特异性还没有在临床中证明其效益。Bempegaldesleukin(NKTR-214)是一种CD122优先结合的IL-2路径的激动剂,旨在通过靶向CD122特异性受体激活T细胞和NK细胞。CD122,也被称为也被称为IL-2受体β(IL.2Rb)亚单位,是一个重要的信号受体,可增加这些效应细胞的扩增。NKTR-214在一项多中心I期临床研究(包括2名BC患者)展现了临床效果,包括肿瘤减少和持续的疾病稳定。一项研究将NKTR-214与抗PD-1抗体nivolumab联合在转移性三阴性BC(TNBC)患者中显示出令人鼓舞的结果,但仍缺乏关于HER2阳性BC患者的数据。
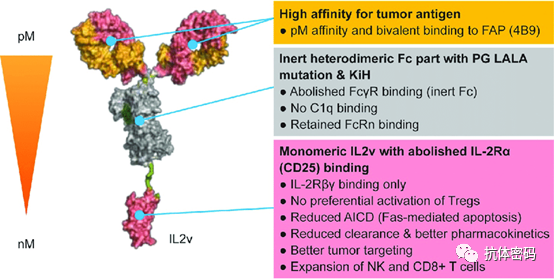
RO6874281是一个重组的融合蛋白,由一个靶向成纤维细胞激活蛋白-α(FAP)的抗体和与一种具有潜在免疫刺激和抗肿瘤活性的IL-2(IL-2v)的变异组成。FAP是一种表达在各种癌症细胞上的蛋白质。在给予RO6874281后,mAb分子会识别并附着在FAP上,从而使IL-2集中在表达FAP的肿瘤组织中。随后,融合的IL-2分子可以激活局部免疫反应并刺激NK细胞。IL-2v不能与IL-2 Ra结合,也不能激活调节性Tregs。BP29842研究正在评估RO6874281与曲妥珠单抗联合应用于HER2阳性的转移性疾病患者的安全性、耐受性和早期活性。目前,RO6874281正作为单药在对晚期和/或转移性实体瘤患者进行研究,初步结果显示,在血液和肿瘤样本中,当IL-2v无法IL-2Ra结合时,其可以刺激效应T和NK的快速扩张,而不会激活Tregs细胞。
IL-12
白细胞介素-12(IL-12)最初被命名为NK细胞刺激因子,由APC细胞产生,如DCs、单核细胞和巨噬细胞。它通过增加IFN-γ的产生而发挥作用。IFN-γ是IL-12在NK和T细胞中作用的最有力的媒介;刺激NK细胞、CD8þ和CD4þ T细胞的成熟和发挥细胞毒性;以及增强针对肿瘤细胞的ADCC效应。低剂量IL-12可以降低CD56的荧光强度,并促使更成熟的CD56dimCD16þ和CD56dimKIRþ NK细胞的扩增。研究表明,曲妥珠单抗和IL-12共刺激NK细胞可以产生比单独用两种药剂刺激的NK细胞高10倍的IFN-γ。在一项I期临床试验中,曲妥珠单抗与IL-12联合用于HER2þ肿瘤患者,临床疗效与NK细胞产生的IFN-γ具有相关性。一项关于曲妥珠单抗、IL-12和紫杉醇的I期后续试验证实了这些结果。相比之下,临床疗效与研究中入组的患者的ADCC没有相关性。这一发现可能揭示了体外实验无法反应肿瘤微环境中发生的NK细胞细胞毒性活动的真实程度。尽管期望值很高。最初的IL-12临床研究并没有获得足够的结果。在最初的IFN-γ刺激后注射IL-12会导致适应性反应和IL-12诱导的 IFN-g的逐渐下降
IL-15
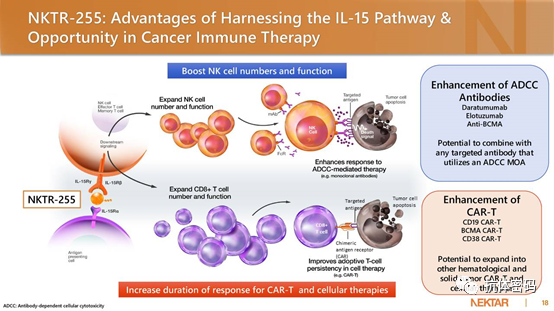
白细胞介素-15(IL-15)具有类似于IL-2的刺激功能,对NK细胞的发展和作用至关重要。IL-15和IL-2只有a链不同,共有b链和γ链。然而,IL-15Ra单独与IL-15结合,其亲和力与IL-2相似。亲和力类似于IL-2Raβγ与IL-2的结合。这种较高的亲和力使NK细胞在相对低的浓度下被激活。在这种相互作用之后,NK细胞会对二次刺激敏感,即所谓的 "引爆"并导致反应的放大。IL-15促进NK细胞做好充分准备,并快速的产生颗粒酶和穿孔蛋白,并且NK细胞的细胞溶解能力在细胞因子之后仍然保留。研究表明,IL-15与曲妥珠单抗同时给药在小鼠模型中引起免疫反应,从而消灭肿瘤并防止转移的发生。 NKTR-255是一种聚合物结合的人IL-15旨在激活IL-15通路,扩大NK细胞并促进记忆性CD8þ T细胞的生存和发展。而不诱导Treg。通过与IL-15Ra/IL-2Rβγ受体复合物,它加强了长期免疫记忆的形成并导致持续的抗肿瘤免疫反应。NKTR-255克服了重组IL-15所面临的快速被清除和频繁的高剂量给药的毒性及使用的挑战。临床前研究表明NKTR-255增强了曲妥单抗在小鼠模型中的抑制肿瘤生长的能力,同时表明它有可能被应用于某些癌症治疗中,以提高肿瘤靶向mAbs的ADCC依赖性治疗活性。
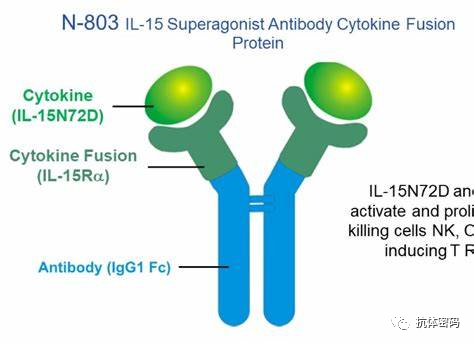
ALT-803(N803)是一种IL-15超级拮抗剂,其将IL-15Ra融合到IgG1的Fc上,与IL-15 (N72D)结合。与IL-15相比,其具有更长的半衰期(25小时与<40分钟),目的是激活ADCC。在一项1期临床试验中,ALT-803对总淋巴细胞和CD8þ T细胞的扩增是不明显,但是,NK细胞的数量却大幅增加。这些数据,加上临床前和临床研究中令人信服的协同作用的证据,提供了将其与临床实践中已有的药物相结合的理由,如抗HER2抗体±Avelumab。
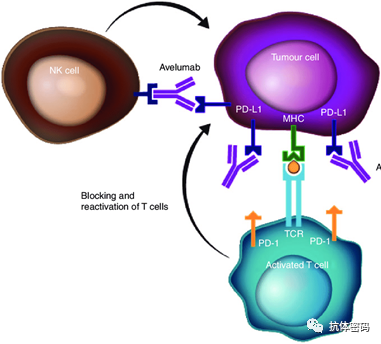
Avelumab
Avelumab是一种全人类IgG1抗PD-L1 mAb,能够引发ADCC。JAVELIN实体肿瘤I期临床试验测试了Avelumab作为单一疗法治疗严重预处理的转移性BC患者,仅有3.0%的ORR。在肿瘤有浸润的免疫细胞表达PDL1þ患者中更高较低的ORR(ORR为16.7%VS1.6%),而且在TNCB中,这种响应的持续时间令人惊讶。然而,在HER2阳性的患者中没有观察到反应(n: 26)。与其他抗PD-L1不同的是,Avelumab保留了其Fc部分和通过结合CD16诱导ADCC的能力。这一机制已经在体外的几个人类肿瘤细胞系中得到证实,特别是在BC细胞系中。Julia和col利用5个TNBC细胞系实验表明,这种效应与PD-L1的表达有关。免疫细胞对Aveluma介导的ADCC内在抵抗力的机制尚不清楚,但可能与IFN-γ诱导的淋巴细胞表面的MHC-I有关(MHC-Ⅰ是一个已知的NK细胞的负面调节)。如前所述,AVIATOR研究(NCT03414658)评估了曲妥珠单抗和长春瑞滨与阿维鲁单抗或阿维鲁单抗加乌洛咪单抗在晚期HER2阳性BC中的作用,并且将会提供更多的信息。
Magrolimab
magrolimab是一种人源化的mAb,可阻断CD47与信号调节蛋白a(SIRPa)的相互作用,从而减少了癌细胞对巨噬细胞的抑制。当Hu5F9-G4(magrolimab)阻断CD47 "不要吃我 "的信号时,它促进了吞噬作用的巨噬细胞。最近的一项临床前研究表明,magrolimab和曲妥珠单抗的组合能消除HER2þ BC细胞,并通过增强巨噬细胞对抗体依赖性的细胞吞噬作用提高疗效。
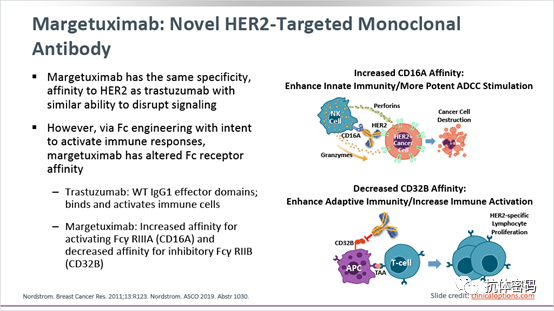
Margetuximab
Margetuximab是靶向HER2第四结构域的单克隆抗体,与曲妥珠单抗(Trastuzumab)不同,该抗体对Fc进行改造(F243L/R292P/Y300L/L235V/P396L),增强抗体对CD16A的结合能力,从而增加抗体介导的ADCC效应,同时该抗体降低了对CD32B的亲合力,以此增强增机体的免疫反应。该药于2020年12月已经被FDA获批,用于联合化疗治疗成人转移性HER2阳性乳腺癌。
改变糖基化增强ADCC
对于几种不同的单克隆抗体,有报道称改变糖基化模式的改变可以用来增加激活FcgR的亲和力,以提高ADCC活性。在Fc结构域的低聚糖中,岩藻糖在决定Fc与FcγRIIIA结合方面起着最大的作用。这些研究导致了缺乏岩藻糖Fc生产方法的发展。Junttila等人证明,从曲妥珠单抗中去除岩藻糖增加其与FcγRIIIa的结合,增强ADCC,与传统的曲妥珠单抗相比,在临床前模型中,其中位PFS增加了一倍以上。
TrasGEX
TrasGEX是曲妥珠单抗的第二代mAb,经过糖优化,以增强ADCC,同时完全保留曲妥珠单抗与HER2抗原结合特性。一项I期临床剂量递增研究已经完成,结果表明其具有良好的安全性,耐受性良好,并在50%的可评估患者中显示出抗肿瘤活性(NCT01409343) 。
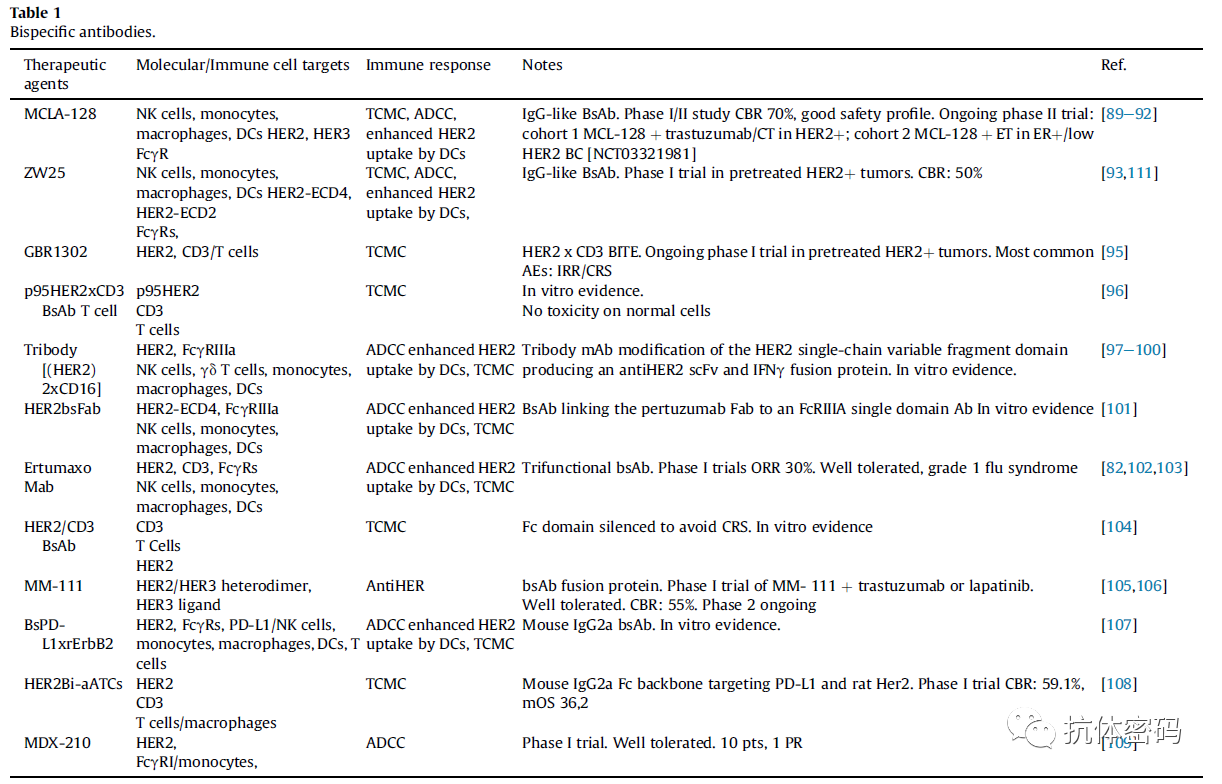
通过工程抗体重定向NK细胞(双特异抗体)
双特异抗体是能够同时靶向两个不同抗原或者靶向同一抗原不同表位的抗体,在靶向HER2治疗BC领域,目前已经有多款双特异抗体正在临床中(下表),其中多数抗体都通过增强ADCC效应以期提高抗体的治疗效果,如靶向HER2/HER3的MCLA-128通过去除岩藻糖增加抗体的活性;靶向HER2不同结构域的ZW25也通过对Fc改造增强抗体的ADCC效应。除了对Fc或者糖基化改造增强ADCC效应外,部分抗体直接靶向CD16,增强NK细胞的活性,如HER2/CD16的Tribody等。
近年来,免疫治疗在肿瘤的治疗中取得了长足的进步,特别是在HER2阳性的BC治疗中。随着研究的深入,研究者发现曲妥珠单抗和培妥珠单抗的ADCC效应在肿瘤的治疗中也发挥了重要作用,而且一些减弱ADCC效应的因素如FcgRIIIa多态性和免疫抑制环境等因素与肿瘤的复发和进展具有一定的关系,因此目前临床中许多研究希望通过多种方式增强ADCC效应,如工程化改造抗体增加抗体Fc与FcγR的结合,通过与免疫检查点抑制剂联用,或者直接靶向NK细胞并激活NK细胞等,增强抗体的治疗效果,并且目前部分临床的项目已经取得了较好的效果。
参考文献
1、Lisa T C Vogelpoel , Dominique L P Baeten, Esther C de Jong et al. Control of cytokine production by human Fc gamma receptors:implications for pathogen defense and autoimmunity. Front. Immunol. 2015
2、Pablo Mand_o,Sergio G. Rivero, Manglio M. Rizzo et al. Targeting ADCC: A different approachto HER2 breast cancer in the immunotherapy era. The Breast 2021
3、相关公司官网




